Программа скат антибиотики что это
Руина О.В. 1, 2 Фурман М.Г. 1 Бельский В.А. 1 Тотмина Т.Б. 1 Конышкина Т.М.
2 Саперкин Н.В. 2 Жукова О.В. 2 Шпрыкова О.Н. 3
1 ФБУЗ «Приволжский Окружной Медицинский Центр» ФМБА России
2 ФГБОУ ВО «Приволжский Исследовательский Медицинский Университет» МЗ РФ
3 ГБУЗ НО «Инфекционная клиническая больница № 2»
Разработаны подходы к антибиотикотерапии в отделении реанимации стационара высоких медицинских технологий, имеющего в своем составе хирургические, онкологические, терапевтические, гинекологические, урологические койки. Показано, что спектр и резистентность микроорганизмов, выявленных в отделении реанимации, отличаются от общебольничной картины.
Выявлены более высокий уровень устойчивости как грамположительной, так и грамотрицательной флоры, более частое по сравнению с остальным стационаром выделение полирезистентных, крайне сложных для терапии штаммов Acinetobacter baumannii. В отделении реанимации достоверно чаще, чем в среднем по стационару, регистрировались метициллинрезистентные штаммы стафилококков и устойчивые к цефалоспоринам грамотрицательные микроорганизмы. Выявленные особенности требуют разработки дифференцированных алгоритмов стартовой антибиотикотерапии для отделения реанимации с участием врача – клинического фармаколога. Не могут быть рекомендованы к рутинному использованию цефолоспорины II и III поколений, фторхинолоны, пенициллины, которые с успехом применяются в ряде других отделений клиники. Использование в реанимационном отделении антибактериальных препаратов резерва (карбапенемов в комбинации с ванкомицином, тигециклина, полимиксина, фосфомицина), часто в составе комбинированных схем, может быть оправдано в связи с высоким уровнем антибиотикорезистентности.
Водительский терминал СКАТ

антибиотикорезистентность
реанимационное отделение
стартовая антибиотикотерапия
1. Клиническая фармакология: национальное руководство / Под ред. Ю.Б. Белоусова, В.Г. Кукеса, В.К. Лепахина, В.И.
Петрова. М.: ГЭОТАР-Медиа, 2014. 976 с.
2. Козлов С.Н., Козлов Р.С. Современная антимикробная химиотерапия: Руководство для врачей. 3-е изд.; перераб. и доп. М.: Медицинское информационное агентство. 2017. 400 с.
3. Гельфанд Б.Р., Яковлева С.В. Савельева В.С. Стратегия и тактика применения антимикробных средств в лечебных учреждениях России: Российские национальные рекомендации. М: Компания «БОРГЕС», 2012. 92 с.
4. Распоряжение Правительства Российской Федерации от 25.09.2017 № 2045-р «Стратегия предупреждения распространения антимикробной резистентности в Российской Федерации на период до 2030 года». [Электронный ресурс]. URL: https://www.garant.ru/products/ipo/prime/doc/71677266/ (дата обращения: 23.07.2020).
5. Руина О.В., Жукова О.В., Хазов М.В., Борисов В.И., Мельниченко О.В., Новикова Р.А., Гнучина Д.С., Хорошавина Е.С. Взаимосвязь потребления антибиотиков и локальной микробиоты // Современные проблемы науки и образования. 2020. №1.; URL: http://science-education.ru/ru/article/view?id=29488 (дата обращения: 23.07.2020).
16 04 3 канал 2 Стратегия контроля антимикробной терапии СКАТ
6. Бабаев С.Ю. Руина О.В., Митрофанова Н.Н., Строганов А.Б. Сравнительный мониторинг антибиотикорезистентности микрофлоры многопрофильных стационаров в городах Пенза и Нижний Новгород // Медицинский альманах. 2016. № 3(43). С. 67-70.
7. Витик А. А., Суханова Н. В., Пыленко Л. Н. Этиология и антибиотикорезистентность возбудителей нозокомиальных инфекций в гнойно-септическом отделении анестезиологии и реанимации. // Университетская медицина Урала 2017. №2. С. 40-44.
8. Программа СКАТ (Стратегия Контроля Антимикробной Терапии) при оказании стационарной медицинской помощи. Российские клинические рекомендации. М., 2017. 132 с.
9. Руина О.В., Васильева Н.П., Сухачева Н.Н., Конышкина Т.М., Саперкин Н.Н., Чуева Т.О., Мельниченко О.В., Бязрова А.В., Храмов Д.В., Токарева А.С. Микробиологический мониторинг в многопрофильном стационаре и пути оптимизации затрат на антибактериальные препараты // Медицинский альманах. 2013. № 5(29). С. 187–190.
10. Сорокина Ю.А., Занозина О.В., Ловцова Л.В., Столярова В.В., Борисова К.А., Жуков И.А. Гипогликемия и гипергликемия: потенциальные риски полипрагмазии при сахарном диабете 2-го типа в госпитальных условиях// Медицинский совет. 2018. № 4. С. 112-115.
11. Руина О.В., Хазов М.В., Борисов В.И., Конышкина Т.М., Жукова О.В., Зайцева Е.И., Дудукина Ю.А., Козлова Е.А. Взаимосвязь структуры назначаемых препаратов с коморбидностью у пациентов с сахарным диабетом 2-го типа на госпитальном этапе // Современные проблемы науки и образования. 2019. № 1. URL: http://science-education.ru/ru/article/view?id=28515 (дата обращения: 23.07.2020).
12. Naber K.G., Bergman B., Bishop M.C. et al. Guidelines on Urinary and Male Genital Tract Infections European Association of Urology. 2011. 115 p.
13. Перепанова Т.С. Федеральные клинические рекомендации «Антимикробная терапия и профилактика инфекций почек, мочевыводящих путей и мужских половых органов – 2015 г.» // Терапевтический архив. 2016. № 4 (88). С. 100–104.
Антибиотикорезистентность – неизбежное биологическое явление, связанное с высокими способностями микроорганизмов к адаптации. Механизмы развития антибиотикорезистентности зависят от вида микроба и от химической структуры антибиотика [1]. Устойчивые к терапии возбудители представляют опасность не только для пациента, но и для всего стационара и общества в целом, это явление носит название «концепция параллельного ущерба» [2, 3]. Актуальность проблемы устойчивости микробных патогенов к антибактериальным препаратам отмечена на правительственном уровне [4].
На сегодняшний день бесспорным считается тот факт, что планирование применения антимикробных препаратов должно осуществляться с учетом не только глобальных, общемировых тенденций, но и локальной картины микробной резистентности в условиях города, стационара, отделения, чему посвящено немало исследовательских работ [5–7]. Факторы риска полирезистентных возбудителей общеизвестны: на сегодняшний день доказано, что свою лепту вносят хирургическое вмешательство, пребывание в домах длительного ухода, в реанимации, использование аппарата ИВЛ, катетеров, инвазивных устройств, парентеральное питание, предшествующая госпитализация, прием антибиотиков в период, предшествующий заболеванию, посещение отделения амбулаторного гемодиализа; в ряде случаев отмечаются случаи устойчивости внебольничной флоры [8, 9]. Отдельный вклад вносят тяжелые сопутствующие хронические заболевания. В первую очередь это сахарный диабет, который влечет не только применение большого количества лекарственных препаратов, в том числе антибактериальных (следствием чего являются связанные с этим лекарственные взаимодействия), но и более частое обращение за медицинской помощью, иммунодефицит, риск инфекционно-гнойных заболеваний, хронической почечной недостаточности [10, 11]. В урологии отягощающими факторами являются хроническая мочевая инфекция, затруднение пассажа мочи, наличие стом и катетеров [12, 13].
Факторы риска полирезистентной флоры в большом количестве представлены в отделении реанимации. Оптимизировать стартовую антибиотикотерапию можно, имея на руках данные локального микробиологического мониторинга – не только по стационару в целом, но и конкретно по реанимационному отделению. На основе полученных данных возможна разработка локальных протоколов антибиотикотерапии при непосредственном участии врача – клинического фармаколога.
Целями настоящего исследования явились изучение микробиологического профиля отделения реанимации, сравнение с общей картиной по больнице, разработка рекомендаций по стартовой антибиотикотерапии реанимационных пациентов.
Материал и методы исследования. Проведен микробиологический мониторинг на базе многопрофильного стационара плановой высокотехнологичной медицинской помощи. Отдельное внимание уделено отделению реанимации. Выявлены превалирующая флора, уровень ее резистентности, проведено сравнение с общебольничными данными.
Стационар на 200 коек включает в себя хирургические, урологические, гинекологическое и терапевтические отделения, а также реанимационное отделение. Проанализированы данные микробной устойчивости патогенов, выделенных из биосубстратов пациентов, за 2018 г. Всего исследовано 885 образцов биоматериала, из них более половины (493 образца) оказались отрицательными, 392 – положительными. В дальнейшем проводился анализ только положительных образцов биоматериала. Исследовались моча, кровь, раневое отделяемое, мокрота, трахеальный аспират, материал бронхо-альвеолярного лаважа, посев со слизистой носа, ротоглотки, половых органов, транссудаты и экссудаты, отделяемое дренажей, ликвор. 182 посева (46%) из числа положительных микробиологических исследований приходились на отделение реанимации.
По нозологической характеристике пациентов определено, что в онкологическом хирургическом отделении около трети пациентов составляли больные с опухолями кишечника, 25% – с опухолями печени, около 20% – с опухолями поджелудочной железы, реже встречались опухоли желудка, пищевода. В отделении трансплантации органов более трети пациентов составили больные с хроническими заболеваниями почек, хронической почечной недостаточностью.
Реже встречались пациенты с патологией печени, поджелудочной железы. В отделении рентгенохирургических методов лечения преобладали пациенты с ИБС, нарушениями ритма. В гинекологическое отделение наиболее часто (в 45% случаев) госпитализировались пациентки с опухолями матки. Госпитализации по поводу опухолей яичников, трубно-перитонеального бесплодия, воспалительных заболеваний женских половых органов, эндометриоза, опущения гениталий, внематочной беременности составили по 5–10%. В урологические отделения 2/3 пациентов госпитализировали с онкологическими заболеваниями мочевого пузыря, почек, предстательной железы, примерно 30% составили пациенты с мочекаменной болезнью, гидронефрозом, около 3% пациентов госпитализировались с целью проведения операций на уретре, половом члене, в 4% случаев – с целью орхэктомии.
В терапевтические отделения направлялись пациенты с кардиологической, эндокринной, ревматологической патологией, а также с воспалительными заболеваниями нижних дыхательных путей, хроническим обструктивным бронхитом, бронхиальной астмой, заболеваниями желудочно-кишечного тракта, анемиями. Таким образом, можно видеть, что нозологический круг пациентов достаточно разнообразен.
Все прооперированные пациенты переводились в отделение реанимации в первые сутки после операции, если того требовало их состояние, и при необходимости находились там далее. Терапевтические пациенты госпитализировались в реанимационное отделение лишь при декомпенсации хронического заболевания или при возникновении острого состояния. Пациенты отделения гинекологии и отделения рентгенохирургических методов лечения переводились в реанимацию реже, чем после обширных онкологических или урологических операций. Трансплантация солидных органов всегда требовала реанимационного пособия.
В качестве материала для микробиологического исследования в данной работе использовались биосубстраты, полученные от пациентов. Идентификацию возбудителей проводили по общепринятой методике. Для статистической обработки материала использовали программу WHONET 5.4, математический комплекс методик программного обеспечения Excel. Оценка значимости различий проводилась по t-критерию Стьюдента, статистически значимыми различия признавались при р
Результаты исследования и их обсуждение. В результате анализа микробиологического исследования биосубстратов, полученных от пациентов, выяснилось, что в стационаре преобладала грамотрицательная флора.
В отделении реанимации определена тенденция к более частому выделению грамотрицательных микроорганизмов (табл. 1), достоверной закономерности не выявлено (t-критерий Стьюдента 3,1, p=0,055), так как грамотрицательная флора достоверно превалирует над грамположительной во всей больнице (t-критерий Стьюдента 31,8, p=0,02).
Структура выделения микробных патогенов в стационаре и в отделении реанимации, данные за 2018 г.
Доля грамположительных патогенов
Доля грамотрицательных патогенов
Источник: science-education.ru
Программа СКАТ: сохранить антибиотики для будущих поколений
Несмотря на воскресный день и прекрасную погоду за окном желающих попасть на сегодняшний семинар более, чем достаточно. В актовом зале Республиканской больницы № 2-Центра экстренной медицинской помощи — врачи общей практики, кардиологи, анестезиологи-реаниматологи, хирурги, терапевты, клинические фармакологи, неврологи, педиатры из республиканских, городских и районных больниц, в основном молодые.
От имени главного врача больницы приветствовал участников семинара его заместитель по лечебной части Александр ПЕТРОВ.
Открыл семинар д.м.н., заведующий кафедрой анестезиологии, реаниматологии и интенсивной терапии с курсом скорой медицинской помощи ФПОВ МИ ФГАОУ ВО «Северо-Восточный федеральный университет им. М.К. Аммосова» Министерства образования и науки РФ, руководитель Республиканского центра мониторинга антибиотикорезистентности Александр ПОТАПОВ. Александр Филиппович представил гостей семинара и ознакомил собравшихся с состоянием мониторинга антибиотикорезистентности в Республике Саха (Якутия).
Д.м.н., профессор кафедры госпитальной терапии № 2 Первого МГМУ им. И.М. Сеченова, Президент межрегиональной общественной организации «Альянс клинических химиотерапевтов и микробиологов» Сергей ЯКОВЛЕВ выступил с двумя докладами: «Новые Российские рекомендации СКАТ для стационаров России» и «Актуальные проблемы диагностики и антибактериальной терапии инфекций, вызванных полирезистентными грамположительными и грамотрицательными микроорганизмами».
Справка
Антибиотикорезистентность — это устойчивость микробов к антимикробным химиопрепаратам. Антибиотикорезистентность коснулась всех видов микроорганизмов и является основной причиной снижения эффективности антибиотикотерапии. Проблема антибиотикорезистентности стала особо актуальной и тревожной в XXI веке. Решение проблемы лечения в стационаре инфекций, вызванных полирезистентными бактериями, связано в основном не с ожиданием появления новых антибиотиков, а с разработкой и внедрением решительных и адекватных мер по сдерживанию антибиотикорезистентности.
Я успела поговорить с профессором ЯКОВЛЕВЫМ до начала семинара.
— Сегодня мы обсуждаем проблему рационального приема антибиотиков и сложности с этим связанные, — сказал Сергей Владимирович. — Развивается антибиотирезистентность, то есть микробы, на которые направлено действие тех или иных антибиотиков, становятся к ним устойивыми. Причем, с каждым годом эта проблема нарастает лавинообразно, и мы рискуем оказаться без эффективной антибиотикотерапии. Сегодняшний семинар посвящен госпитальным проблемам, и мы будем говорить с врачами о программе СКАТ, чтобы сохранить антибиотики для будущих поколений.
— Антибиотики можно свободно купить в любой аптеке, есть люди, которые принимают их даже без обращения к врачу, считая, что хуже не будет, — говорю я профессор ЯКОВЛЕВУ, на что он мгновенно реагирует:
— Будет хуже, потому что антибиотик способствуют развитию резистентных микробов, которые человек после приема антибиотика будет носить в себе и распространять, и прежде всего своим близким, а когда будет ситуация и понадобится антибиотик, он может оказаться неэффективным. Антибиотики нужно принимать только по назначению врача! Массовое применение антибиотиков и свободная продажа их в аптеках — это весомый вклад в антибиотикорезистенцию.
Справка
Программа СКАТ (Стратегия Контроля Антимикробной Терапии) реализуется в России с 2011 года. Как показала реальная клиническая практика, благодаря программе СКАТ можно оптимизировать применение антибиотиков при участии тех специалистов, которые имеют возможность влиять в стационаре на принятие решений по стратегическим и тактическим вопросам использования антибиотиков — главные врачи и заместители главного врача ЛПУ, клинические фармакологи, микробиологи, госпитальные эпидемиологи, ведущие специалисты терапевтических и хирургических направлений.
О практических шагах реализации программы СКАТ в стационаре, оценке эффективности внедрения СКАТ с позиций рационализации антимикробной терапии, контроля инфекций, связанных с оказанием медицинской помощи и сдерживания резистентности говорил на семинаре д.м.н., доцент кафедры анестезиологии и реаниматологии ИУВ ФГБУ «НМХЦ им. Н.И.Пирогова» Минздрава России, врач анестезиолог-реаниматолог, главный врач стационара НМХЦ им. Н.И.Пирогова Виталий ГУСАРОВ.
— Антибиотикорезистентность — одна из глобальных проблем в медицине на сегодняшний день, — сказал Виталий Геннадьвич, — мы сталкиваемся с ситуацией, когда практикующему врачу невозможно выбрать эффективную схему антибиотикотерапии и помочь больному. К сожалению, все чаще эта проблема приводит к тому, что наши пациенты погибают от тяжелых инфекций. Сегодняшний семинар мы проводим, чтобы помочь практикующему врачу в правильном принятии решения, когда он сталкивается с пациентом с тяжелой инфекцией, что он должен сделать в данной ситуации, особенно если больной находится в реанимации. Я сам анестезиолог-реаниматолог, поэтому не понаслышке знаю, как бывает сложно помочь пациенту.
После каждого выступления участники семинара могли принять участие в дискуссиях, задать вопросы и высказать свое мнение.
— Как вам сегодняшний разговор? — спросила я сидевших рядом молодых врачей.
— Очень своевременно и полезно, — ответили ребята.
Источник: www.pirogov-center.ru
Медицина против резистентности
Пандемия COVID-19 вывела на новый уровень проблему резистентности патогенов к антибактериальным средствам. Из-за тяжести течения индуцируемой коронавирусом бактериальной пневмонии врачи по всему миру активизировали назначение антибиотиков — нередко от своевременности и корректности их применения зависит жизнь пациента, особенно в пожилом возрасте.
Российский опыт применения антибактериальных препаратов во время пандемии коронавируса изучил коллектив ученых из ФГБОУ ВО Саратовский ГМУ им. В. И. Разумовского Минздрава России во главе с Н.А. Кароли. Свои выводы исследователи описали в научной статье «Антибактериальная терапия пациентов с COVID-19 на амбулаторном и стационарном этапах» 1 , опубликованной в журнале «Антибиотики и химиотерапия» (2022). Мы изучили их работу, чтобы предоставить вам ее краткий обзор и несколько практических советов о том, как работать с нерациональным подходом пациентов к использованию антибактериальных средств.
Цель и методология исследования
Целью исследования стала оценка частоты и характера назначения антибиотиков госпитализированным пациентам с подтверждённым COVID-19.
Для этого исследователи п ровели ретроспективный анализ отобранных методом случайной выборки 190 стационарных карт пациентов с подтверждённым COVID-19, находившихся на лечении в различных инфекционных отделениях в сентябре и октябре 2020 года. Для точности показателей из выборки исключили карты 30 больных, которые при поступлении имели показания для назначения антибактериальной терапии: хирургические патологии, обострения хронических инфекционных заболеваний и т. д. Статистическую обработку данных ученые проводили на компьютере с использованием специальной программы SPSS 26.
Результаты и выводы исследования
До госпитализации 109 пациентов уже применяли антибиотики амбулаторно (причем некоторые — по два препарата последовательно или одновременно). Несмотря на то, что амбулаторно антибактериальная терапия проводилась более чем половине пациентов, стационарно антибиотики при поступлении были назначены всем, кроме одной пациентки.
По данным авторов исследования, в стационаре наиболее часто назначаемыми антибиотиками были макролиды (97 чел), преимущественно азитромицин . На втором месте по частоте назначения оказались респираторные фторхинолоны (86 чел), преимущественно левофлоксацин . В большинстве случаев эти препараты назначались в сочетании с цефалоспоринами третьего или четвёртого поколений.
Комбинированные антибактериальные препараты (цефалоспорины 3–4 поколения + сульбактам) назначены 57 пациентам. В ряде случаев были назначены резервные антибактериальные препараты: карбапенемы (8 пациентов) и ванкомицин (5 человек).
Как следует из данных исследования, большинство пациентов получали более одного антибиотика: два препарата были назначены в 54% случаев, три — 21%, четыре — 7%; пять антибиотиков получали двое, шесть — один.
В случае применения одного антибиотика (26 пациентов) назначались:
- азитромицин (9 человек)
- цефалоспорины 3 поколения (7 человек)
- левофлоксацин (6 человек)
- цефалоспорины 4 поколения (2 человека)
- кларуктам и ванкомицин (по одному пациенту).
Также авторы работы обращают особое внимание на то, что антибактериальная терапия проводилась препаратами всех групп длительное время. Максимальное число дней приёма макролидов (без учёта предшествующей терапии на амбулаторном этапе) — 16 дней, респираторных фторхинолонов — 22 дня, цефалоспоринов 3 поколения — 19 дней, цефалоспоринов 4 поколения — 17 дней, карбапенемов — 34 дня. В 100% случаев антибактериальные препараты назначались в первые сутки поступления пациентов, и терапия ими продолжалась до момента выписки из стационара.
Согласно рекомендациям, назначение антибактериальных средств у пациентов с COVID-19 оправдано только при наличии убедительных признаков бактериальной инфекции. Однако, по данным стационарных карт, в динамике наблюдения документированное бактериальное осложнение было зафиксировано только у одной пациентки! У остальных наличие бактериальной инфекции и её возможный источник определены не были.
В результате авторы статьи приходят к следующим выводам: « Таким образом, по данным нашего исследования, частота назначения антибактериальных (АБ) препаратов, включая применение нескольких АБ, превышает частоту их применения в большинстве зарубежных исследований. Назначение АБ происходит сразу же при поступлении пациента в стационар, что подтверждает мысль о том, что врачи часто назначают антибиотики эмпирически, до подтверждения бактериальных осложнений. Чрезмерное использование противомикробных препаратов увеличивает риск развития мультирезистентности внутрибольничных инфекций, которые связаны с неблагоприятными клиническими исходами ».
Где брать информацию о рациональной антибиотикотерапии
В открытом доступе имеются заслуживающие доверия источники по рациональной антибиотикотерапии от экспертов. В том числе эти:
- «Стратегия и тактика рационального применения антимикробных средств в амбулаторной практике. Евразийские клинические рекомендации». Авторы: МОО «Альянс клинических химиотерапевтов и микробиологов», Российское общество акушеров-гинекологов, МОО «Альянс оториноларингологов».
- « Программа СКАТ (Стратегия Контроля антимикробной Терапии) при оказании стационарной медицинской помощи. Российские клинические рекомендации». Авторы: МОО «Альянс клинических химиотерапевтов и микробиологов», Российская ассоциация специалистов по хирургическим инфекциям, Национальная ассоциация специалистов по контролю инфекций, связанных с оказанием медицинской помощи и др.
Типичные ситуации на приеме у врача
Врачам часто приходится объяснять настойчивым пациентам азы медицинских знаний, чтобы убедить их не применять антибиотики. Рассмотрим ряд ситуаций подобного рода, связанных с антибиотикотерапией:
Пациент: Доктор, выпишите мне рецепт на хороший антибиотик. Хочу пропить курс для профилактики — у меня все родственники тяжело болеют ОРВИ.
Врач: Принимать такие препараты для профилактики обычной ОРВИ нет необходимости. Действительно, превентивное лечение антибиотиками применяют в борьбе с некоторыми тяжелыми инфекциями: например, препарат бициллин используют при контакте с больными сифилисом 2 , а цефалоспорины II-III поколения — для профилактики болезни Лайма после укуса клеща 3 . Помимо этого, профилактическое использование антибиотиков идёт в хирургии для предотвращения развития раневых инфекций. Если же вы пообщались с человеком, больным ОРВИ, то принимать антибактериальные средства «для профилактики» бессмысленно. Вирусные болезни антибиотиками не лечатся и точно не профилактируются. А вот средства для укрепления иммунитета сейчас очень уместны.
Пациент: Как антибиотик может помогать бактериям? Он же создан, чтобы их убивать!
Врач: Бактерии, как и любые живые существа, адаптируются к внешним угрозам. Зачастую в битве с лекарством погибают не все патогены — малая доля выживает, меняя конфигурации своих белков и так далее. Чем чаще и дольше мы используем антибиотики, тем больше «учатся» бактерии. И тем выше риск селекции устойчивых штаммов и генов устойчивости, которыми бактерии могут обмениваться друг с другом даже среди разных видов. Это чревато страшными, неизлечимыми бактериальными инфекциями в будущем.
Пациент : Почему все антибиотики рецептурные? Это же не психотропные вещества!
Врач: Степень угрозы резистентности инфекций к антибиотикам не менее масштабна, чем проблема зависимости от психоактивных веществ. Безответственное применение этих препаратов может привести к тому, что врачам будет трудно вылечить даже привычные болезни, наподобие пневмонии или конъюнктивита. Для того, чтобы ограничить самовольное «необязательное» применение антибиотиков, эти препараты являются рецептурными.
Пациент : Хочу пропить два вида антибиотиков параллельно — чтобы наверняка!
Врач : Я не выпишу вам рецепт на два антибиотика, показаний к этому нет. Кроме того, у каждого препарата свой список побочных эффектов, а вы хотите сделать из двух список один длинный.
- Кароли Н. А., Апаркина А. В., Григорьева Е. В., Магдеева Н. А., Никитина Н. М., Смирнова Н. Д., Реб- ров А. П. Антибактериальная терапия пациентов с COVID-19 на амбулаторном и стационарном этапах.Антибиотики и химиотерапия. 2022; 67: 1–2: 24–31. doi: 10.37489/0235-2990-2022-67-1-2-24-31.
- Клинические рекомендации. Сифилис . Министерство здравоохранения Российской Федерации. Год утверждения: 2020.
- Клинические рекомендации. Болезнь Лайма . Некоммерческое партнерство «Национальное научное общество инфекционистов» (ННОИ).
Источник: medznanie.ru
Эффективные лекарства от простатита у мужчин
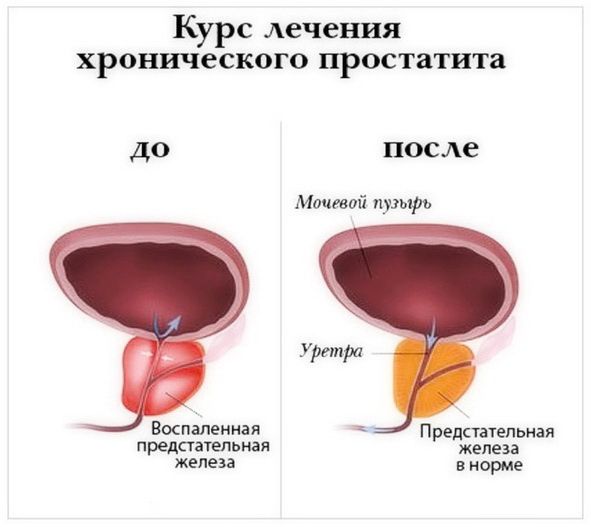
Простатит неодинаково протекает у разных мужчин. Какие-то симптомы бывают более выраженными, какие-то отсутствуют. Большое значение имеет стадия болезни, наличие гиперплазии предстательной железы или аденомы. Врачи учитывают, впервые развилось воспаление или уже имеется стаж.
Подобрать лечение простатита у мужчин, найти самые эффективные средства для каждой стадии простатита может только врач-уролог, после обследования и получения результатов анализов.
Тем не менее ориентироваться в средствах для лечения простатита должен каждый, кто столкнулся с этой проблемой.
Виды лекарств от простатита у мужчин
Урологи применяют несколько групп препаратов.
- Антибиотики — самыми лучшими при этой болезни остаются фторхинолоны (Офлоксацин, Таваник) и макролиды (Вильпрафен).
- Противовоспалительные — Индометацин, Диклофенак, Кетотифен.
- Блокаторы адренорецепторов типа альфа-1 — Омник.
- Лекарства на основе экстракта простаты — Простатилен, Витапрост, Простакор, Сампрост, Уропрост.
- Растительные препараты — Простамол Уно, Простагут форте, Простанорм.
Антибиотики борются с инфекцией в мочевом тракте, все прочие средства снижают воспаление, уменьшают отёк и боль, облегчают отхождение мочи, улучшают кровоснабжение половых и мочевыводящих органов.
Существует масса гомеопатических средств от простатита и потенции, производные интерферона, которые в статье не рассматриваются. Их польза не доказана в исследованиях.
Каким должно быть лучшее средство от простатита у мужчин
Лечение, назначенное врачом, должно достигать следующих целей:
- уничтожение вредных бактерий;
- снятие воспаления;
- ликвидация застойных явлений в простате;
- улучшение иммунитета;
- восстановление нормального мочеиспускания;
- улучшение потенции и предотвращение эректильной дисфункции.
Единственного препарата, который в полной мере отвечает всему перечисленному, нет. Поэтому урологи прописывают приём 2–3 препаратов, подобранных индивидуально в каждом случае. Лекарства сочетают с массажем, физкультурой, физиопроцедурами.
Для лечения простатита у мужчин самыми эффективными средствами считаются ректальные свечи, поскольку поставляют лекарство к железе, минуя печень и создают в тканях высокую лечебную концентрацию.
Топ-5 эффективных средств для лечения простатита
Эти препараты обладают комплексным действием, проверены в клинической практике.
Витапрост
Свечи и ампульный препарат экстракта простаты. Эффективен при остром и хроническом воспалении, поскольку в состав лекарства входит антибиотик.
Лонгидаза
Бактерицидным действием не обладает, назначается вместе с антибиотиком. Подходит в хронических случаях, когда уже появился воспалительный фиброз в органе, спайки, разрастание ткани простаты. Результативна при болезни Пейрони.
Простатилен
Инъекции и ректальные свечи. В сочетании с антибактериальным средством снимает воспаление, нормализует мочеиспускание, улучшает эрекцию.
Простамол Уно
Растительный препарат. Выпускается в капсулах. Уменьшает боли, восстанавливает ток мочевой струи, нормализует потенцию.
Простанорм
Лекарство из растительного сырья. Применяется больше для профилактики, продления ремиссии при хроническом процессе. Имеет небольшой антибактериальный эффект, убирает боль, стимулирует иммунитет, улучшает кровоснабжение железы и отток мочи.
При снижении тонуса мочевыводящей системы врачом по рецепту назначается Омник. В осложнённых случаях при аденоме простаты может потребоваться применение финастерида для регуляции баланса тестостерона.
Хорошо себя зарекомендовали как лекарства от простатита недорогие Ихтиоловые свечи, ампульный Простакор.
Недопустимо самостоятельное применение медикаментов без учёта бактериальной флоры и стадии болезни. Терапия острого простатита под присмотром врача убережёт от осложнений и перехода в хроническую форму.
Для назначения лечения обращайтесь к урологу клиники Dr. AkNer — запишитесь на прием, воспользовавшись формой на сайте или позвонив в нашу клинику по телефону 8 (495) 098-03-03 или 8 (926) 497-44-44.
Меню раздела
- Наши врачи
- Запись на прием
- Онлайн консультация
- Пациентам
- Отзывы
- Задать вопрос урологу
- Акции и спецпредложения
- Новости клиники
- Вакансии
- Статьи и публикации
- Лицензии
Источник: drakner.ru