Цель исследования. Оценка информативности программы пренатальной диагностики синдромов Дауна и Эдвардса в I триместре у пациенток с осложненным течением беременности на фоне гормональной терапии.
Материал и методы. Обследованы в сроки 9–12 нед 505 беременных, получавших гормональную терапию по поводу угрозы прерывания беременности, и 78 женщин с нормально протекающей беременностью. Использованы неинвазивные методы: ультразвуковое исследование, биохимический скрининг, программное обеспечение для оценки рисков патологии плода (компьютерный анализ) и инвазивные – трансабдоминальный хориоцентез или трансцервикальная биопсия хориона для определения кариотипа эмбриона. Статистическая обработка полученных данных проведена с использованием компьютерной программы Excell.
Результаты исследования. У 41,4—51,8% женщин основной группы и 46,1% контрольной были выявлены отклонения от нормативных показателей. При этом статистически значимых различий в этих показателях в зависимости от принимаемого лекарственного препарата женщинами основной группы не выявлено. Группу риска составили соответственно 7 и 3,8% женщин.
ПЕРВЫЙ СКРИНИНГ. Как понять результаты первого скрининга и что делать, если в 3,5 раза повышен ХГЧ.
Основным критерием в формировании группы риска явилось увеличение размеров воротниковой области эмбриона. Хромосомная патология, соответствующая синдрому Дауна, диагностирована только в одном (0,2%) наблюдении в основной группе.
Заключение. Результаты исследования свидетельствуют о том, что осложненное течение беременности и связанный с этим прием гормональных препаратов, по данным неинвазивного скрининга, повышают степень риска рождения ребенка с хромосомной патологией, по данным компьютерной программы, за счет увеличения размеров воротниковой области эмбриона. Однако, по данным инвазивной пренатальной диагностики, частота патологии кариотипа эмбриона у этих женщин не превышает популяционных значений. Таким образом, проведение гормональной терапии при осложненном течении беременности не влияет на показания инвазивной пренатальной диагностики.
Ключевые слова
I триместр беременности
угроза прерывания
гормональная терапия
неинвазивный скрининг
пренатальная диагностика
хромосомная патология
Пренатальная диагностика является наиболее эффективным средством профилактики наследственной патологии плода. Основными методами неинвазивной пренатальной диагностики являются ультразвуковое исследование (УЗИ) и определение уровней сывороточных маркеров. В I триместре беременности (9–13 нед) таковыми являются свободная β-субъединица хорионического гонадотропина человека (свободная β-ХГЧ) и ассоциированный с беременностью белок плазмы крови (РАРР-А) [2]; во II триместре (16–20 нед) – молекула ХГЧ, альфа-фетопротеин (АФП), свободный эстриол (Е3) и 17-гидроксипрогестерон (17-ОП) [3].
В настоящее время разработана система неинвазивной пренатальной диагностики трисомии 18-й
и 21-й хромосом (синдром Эдвардса и синдром Дауна соответственно) у эмбриона в I триместре
беременности, основанная на предварительной компьютерной обработке данных о концентрации свободной β-ХГЧ, РАРР-А, величины носовой кости и воротниковой области эмбриона, его крестцово-теменного размера [4, 11]. В результате обработки этой информации рассчитывют риск наличия у эмбриона синдрома Дауна и синдрома Эдвардса. При значении риска выше 1:250 проводят инвазивную пренатальную диагностику.
Патологические изменения плода, выявляемые при скрининге 1-го триместра беременности
Однако, согласно данным литературы, осложненное течение беременности, особенно наступившей в результате использования вспомогательных репродуктивных технологий, а также лекарственная терапия могут оказывать определенное влияние на концентрацию сывороточных маркеров [1, 7, 8]. В результате этого возникает проблема интерпретации риска наличия у эмбриона синдрома Дауна и синдрома Эдвардса.
В связи с вышеизложенным, целью настоящего исследования явилась оценка информативности
программы пренатальной диагностики синдромов Дауна и Эдвардса в I триместре у пациенток с осложненным течением беременности на фоне гормональной терапии.
Материал и методы исследования
Обследованы 505 беременных женщин в возрасте от 21 до 35 лет в сроке беременности 9–12 нед.
Все женщины получали гестагенные (прогестерон, прогенова, утрожестан, норколут, дюфастон)
и/или глюкокортикоидные прапараты (дексаметазон, метипред, преднизолон). Лекарственные
средства назначали как изолированно, так и в различных сочетаниях. Контрольную группу
составили 78 женщин с нормально протекающей беременностью. Этим женщинам гормональная терапия не проводилась. Исход беременности был установлен у всех обследованных женщин.
Всем женщинам проводили УЗИ и одновременно анализ образцов крови. Исследовали только
те показатели, которые были необходимы для проведения компьютерного анализа. При УЗИ получали данные о крестцово-теменном размере эмбриона и размере его воротниковой области. В сыворотке образцов крови определяли концентрацию свободной β-ХГЧ и РАРР-А на автоматическом иммунофлуоресцентном анализаторе Delfia Xpress фирмы Perkin Elmer, Финдляндия.
Полученные результаты обрабатывали с помощью компьютерной программы Life Cycle этой же фирмы. В программу вносили некоторые анамнестические данные и вышеуказанные лабораторные показатели. Нормативными считали концентрации маркеров в диапазоне 0,5– 2,0 МоМ, размер воротникового пространства до 2 мм и степень риска – выше 1:250. У 40 женщин (37 основной группы и 3 контрольной) с высоким риском рождения ребенка с хромосомной патологией установлен кариотип эмбриона с использованием стандартной техники [10].
Результаты исследования и обсуждение
В контрольной группе, которая была представлена 78 женщинами с нормально протекающей беременностью, закончившейся рождением нормальных детей, отклонения концентраций сывороточных маркеров от нормативного диапазона были выявлены у 36 (46,1%) женщин.
Однако риск рождения ребенка с хромосомной патологией, рассчитанный с помощью компьютерной программы, был установлен только у 3 (3,8%) женщин. У всех этих женщин при УЗИ было отмечено увеличение размеров воротниковой области эмбриона свыше 2 мм. При исследовании кариотипа эмбрионов патологии не выявлено.
Из 505 обследованных женщин у 156 (31%) беременность протекала с угрозой прерывания в I триместре. Отмечались кровянистые выделения из половых путей и в ряде наблюдений, по данным эхографии, наличие гематом.
В таблице 1 представлены данные об особенностях отклонения от норматива таких показателей,
как размер воротниковой области эмбриона, концентрации свободной β-ХГЧ и РАРР-А в периферической крови беременных. Именно эти показатели являются основой для компьютерной оценки риска наличия у эмбриона синдрома Дауна. Согласно результатам компьютерной обработ-
ки данных, риск наличия у эмбриона синдрома Дауна, превышающий пороговые значения 1:250,
был обнаружен у 37 женщин, что составило 7,3%. Угроза прерывания беременности у них отмеча-
лась в 46,0% случаев.
Таблица 1. Отклонения анализируемых показателей в группе обследованных женщин (n=505).
Концентрация свободной β-субъединицы ХГЧ превышала 2 МоМ у 82 (16,2%) пациенток. Угроза
прерывания беременности при этом отмечалась в 35,0% случаев. Концентрация РАРР-А была
ниже 0,5 МоМ у 43 женщин. У 14 (33,0%) из них отмечалась угроза прерывания. В 33 (6,5%) случаях размеры воротниковой области эмбриона превышали 2 мм. В формировании группы риска удельный вес этого показателя составил 89,2%. У 14 (42,0%) пациенток этой группы также отмечалась угроза прерывания беременности.
Одновременное увеличение размера воротниковой области и повышение концентрации свободной β-ХГЧ обнаружено в 5 случаях, у 3 (60,0%) из этих женщин была угроза прерывания беременности. Снижение концентрации РАРР-А ниже 0,5 МоМ в сочетании с размерами воротниковой области более 2 мм зафиксировано в 7 наблюдениях. В этой группе угроза прерывания беременности была только у одной женщины (табл. 1). Таким образом, 41,0% обследованных женщин
имели те или иные отклонения анализируемых показателей от норматива. Частота угрозы прерывания у них варьировалась от 14 до 60,0%.
Согласно данным компьютерного анализа, 37 пациенток, имеющих риск наличия у эмбриона синдрома Дауна, были выделены в группу риска. Им была рекомендована и проведена пренатальная диагностика кариотипа эмбриона – трансцервикальная биопсия хориона или трансабдоминальный хориоцентез с последующим цитогенетическим анализом полученного материала. Кроме того, были более детально проанализированы данные об уровнях сывороточных маркеров и размерах воротниковой области (табл. 2).
Таблица 2. Особенности анализируемых показателей у женщин группы риска.
Из 37 женщин у 32 (86,0%) размеры воротниковой области эмбриона превышали 2 мм, концентрация свободной β-субъединицы ХГЧ превышала 2 МоМ в 4 наблюдениях, а концентрация РАРР-А была ниже 0,5 МоМ у одной женщины. При этом в 7 наблюдениях увеличение размеров воротниковой области сочеталось с низким уровнем РАРР-А, а в 5 случаях – с увеличением концентрации свободной β-ХГЧ. Увеличение размеров воротниковой области в сочетании с нормативными уровнями сывороточных маркеров зарегистрировано в 20 (54,1%) случаях (табл. 2). Таким образом, при оценке риска синдрома Дауна у эмбриона, ведущим показателем является увеличения размера его воротниковой области.
Результаты цитогенетического исследования позволили выявить хромосомную патологию, соответствующую синдрому Дауна, у 1 эмбриона пациентки, относящейся к группе риска. У этого
эмбриона величина воротниковой области достигала 4,5 мм, а концентрация в крови беременной
свободной β-ХГЧ составила 9,5 МоМ. Риск составил 1:5. Беременность протекала без угрозы прерывания на фоне приема утрожестана и дексаметазона. В связи с наличием синдрома Дауна у эмбриона беременность была прервана. Остальные 504 женщины родили детей без хромосомных аномалий.
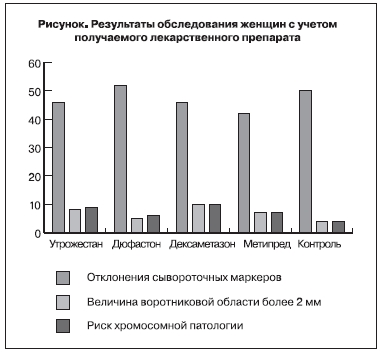
Помимо изучения основной группы в целом, проанализированы показатели с учетом приема гестагенов или глюкокортикоидов. На рисунке в графическом изображении представлены полученные результаты. Частота отклонения концентраций сывороточных маркеров от нормативного диапазона у женщин основной группы, принимавших метипред, составила 41,4%, принимавших дюфастон – 51,8%. В контрольной группе этот показатель составил 46,1%.
Таким образом, согласно результатам статистической обработки, достоверных различий не выявлено. Значимость различий категориальных данных оценивали с помощью χ2-теста с принятием уровня достоверности рс частотой увеличения воротниковой области эмбриона. Поскольку число наблюдений с этим эхографическим признаком в контрольной группе было минимальным, то и частота высокого риска в этой группе была низкой.
По данным литературы, угроза прерывания беременности, гормональная терапия, стимуляция овуляции в программе экстракорпорального оплодотворения (ЭКО) оказывают влияние на концентрацию свободной β-ХГЧ и РАРР-А [7, 9]. Это может затруднять диагностику хромосомной патологии, в частности синдромов Дауна и Эдвардса, проводимых в этот период. Результаты настоящего исследования свидетельствуют о том, что различные отклонения от нормального содержания в крови β-ХГЧ и/или РАРР-А были у 41,4–51,8% женщин основной группы (принимавших гестагенные или глюкокортикоидные препараты с лечебной целью при угрозе прерывания беременности) и у 46,1% женщин контрольной (без гормональной терапии с нормальным течением беременности). Статистически значимых различий в этих показателях в обеих группах, а также в основной, с учетом характера принимаемого лекарственного препарата, не выявлено.
Несмотря на то что у большинства женщин были установлены отклонения концентраций сывороточных маркеров от норматива, высокий риск хромосомной патологии отмечен всего у 7,3% по сравнению с 3,8% в контроле. Высокий риск был только у тех женщин, у которых при эхографии диагностировано увеличение размеров воротниковой области эмбриона. Именно этот маркер являлся ведущим при оценке риска хромосомной патологии.
Хромосомная патология, соответствующая синдрому Дауна, была диагностирована в основной группе в одном наблюдении, т.е. в 0,2% (1 из 505). Эта частота полностью соответствует популяционному нормативу для женщин моложе 35 лет [2]. Частота ложноположительных результатов по синдрому Дауна составила 7,1% (36 эмбрионов женщин группы риска из 505 обследованных), что согласуется с данными литературы [4, 5, 6, 11].
Таким образом, применение гормональной терапии при осложненном течении беременности не влияет на показания к проведению инвазивной пренатальной диагностики, которая на сегодняшний день является основным методом выявления хромосомной патологии плода.
В литературе имеются сообщения о влиянии гормональной терапии на морфологию плода [7, 9]. В настоящей работе увеличение размеров воротниковой области плода у женщин группы риска в определенной степени подтверждают эту точку зрения, однако требуются дальнейшие исследования в этом направлении.
Список литературы
1. Екимова Е.В., Гончарова Е.А., Алексеева М.Л. и др. Хорионический гонадотропин и их свободная
β-субъединица // Пробл. репрод. – 2007. – № 1. – С. 96—98.
2. Некрасова Е.С., Николаева Ю.А., Кащеева Т.К. и др. Внедрение алгоритма комбинированного скрининга хромосомной патологии плода в I триместре беременности. Опыт работы за 4 года // Журн. акуш. и жен. бол. – 2007. – Т. 56. – вып. 1. – С. 28—34.
3. Пренатальная диагностика наследственных и врожденных болезней // Под ред. Э. К. Айламазяна, В.С. Баранова. – М.: МЕДпресс-информ, 2006. – С. 116—124.
4. Bindra R., Heath V., Liao A. . One-stop clinic for assessment of risk trisomy 21 at 11-14 weeks a prospective study of 15030 pregnancies // Ultrasound Obstet.Gynecol. – 2002. – Vol. 20. – P. 219—225.
5. Cicero S., Bindra R., Rembouskos G. et al. Integrated ultrasound and biochemical screening for trisomy 21 using fetal nuchal translucency, absent fetal nasal bone, free betahCG and PAPP-A at 11 to 14 weeks // Prenat.Diagn. – 2003. — Vol. 23, 4. – P. 306—310.
6. Hernandez-Andrade E., Guzman Huerta N., Garcia Cavazos R., Ahued-Ahued J.R. Prenatal diagnosis in the first trimester, whom and how? // Ginecol. Obstet. Mex. – 2002. – Vol. 70. – P. 607—612.
7. Liao A.W., Heath N., Kamelas K. First-trimester screening for trisomy 21 singleton pregnancies achived by assisted reproduction // Hum. Reprod. – 2001. – Vol. 16. – P. 1501—1504.
8. Miller F., Dreux S., Lemeu R. A. Medically assisted reproduction and second trimester maternal serum marker screening for Down syndrome // Prenat. Diagn. – 2003. – Vol. 23. – P. 1073—1076.
9. Orlandi F., Rossi D., Allegra A. First trimester screening with free ¡ – HCG, PAPP-A and nuchal translucency in pregnancies, conceived with assisted reproduction // Prenat. Diagn. – 2002. –Vol. 22.– P. 718—721.
10. Simpson J.L., Elias S. Genetic in obstetrics and gynaecology. – 3rd ed. – Philadelphia: WB Saunders,
2003. – P. 345—455.
11. Spencer K., Spencer C.E., Power M. et al. Screening for chromosomal abnormalities in the first trimester using and maternal serum biochemistry in a one-stop clinic: a review of three years prospective experience /
Об авторах / Для корреспонденции
Источник: aig-journal.ru
Беременность – пренатальный скрининг трисомий I триместра беременности (синдром Дауна)
Неинвазивное исследование, которое на основании определенных лабораторных маркеров и клинических данных позволяет при помощи компьютерной программы рассчитать вероятный риск развития хромосомных болезней или других врожденных аномалий плода.
Синонимы русские
Биохимический скрининг I триместра беременности, «двойной тест» 1-го триместра.
Синонимы английские
Maternal Screen, First Trimester; Prenatal Screening I; PRISСA I (Prenatal Risk Calculation).
Метод исследования
Твердофазный хемилюминесцентный иммуноферментный анализ («сэндвич»-метод), иммунохемилюминесцентный анализ.
Единицы измерения
ММЕ/мл (милли- международная единица на миллилитр), МЕ/л (международная единица на литр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Исключить из рациона жирную пищу за 24 часа до анализа.
- Исключить физическое и эмоциональное перенапряжение в течение 30 минут до анализа.
- Не курить в течение 30 минут до анализа.
Общая информация об исследовании
Болезнь Дауна – хромосомное заболевание, связанное с нарушением клеточного деления (мейоза) при созревании сперматозоидов и яйцеклеток, которое приводит к образованию дополнительной 21-й хромосомы. Частота в популяции – 1 случай на 600-800 родов. Риск хромосомной аномалии увеличивается с возрастом роженицы и не зависит от состояния здоровья матери ребенка, факторов внешней среды. Синдром Эдвардса (трисомии 18) и синдром Патау (трисомии 13) менее связаны с возрастом матери, а популяционная частота составляет 1 случай на 7000 родов. Для точной пренатальной диагностики генетических заболеваний требуются инвазивные процедуры, которые связаны с большой вероятностью осложнений, поэтому для массового скрининга используются безопасные методы исследования, позволяющие выявить низкий или высокий риск хромосомных аномалий и оценить целесообразность дальнейшего обследования.
Для скрининга обязательно учитываются клинические данные (возраст беременной, масса тела, количество плодов, наличие и особенности ЭКО, раса матери, вредные привычки, наличие сахарного диабета, принимаемые лекарственные препараты), данные УЗИ (копчико-теменной размер (КТР) и толщина воротникового пространства (ТВП), длина носовой кости). При наличии данных УЗИ срок беременности рассчитывается по величине КТР, а не по дате последней менструации.
После исследования и расчета риска проводится плановая консультация у врача – акушера-гинеколога.
Результаты скринингового исследования не могут служить критериями для постановки диагноза и поводом для искусственного прерывания беременности. На их основании принимается решение о целесообразности назначить инвазивные методы обследования плода. При высоком риске необходимы дополнительные обследования, в том числе пункция хориона, амниоцентез с генетическим исследованием полученного материала.
Для чего используется исследование?
- Для скринингового обследования беременных, чтобы оценить риск хромосомной патологии плода – трисомии 21 (синдрома Дауна), синдрома Эдвардса.
Когда назначается исследование?
- При обследовании беременных в первом триместре (анализ рекомендован на сроке беременности 10 недель – 13 недель 6 дней), особенно при наличии факторов риска развития патологии:
- возраст старше 35 лет;
- невынашивание и тяжелые осложнения беременности в анамнезе;
- хромосомные патологии, болезнь Дауна или врожденные пороки развития при предыдущих беременностях;
- наследственные заболевания в семье;
- перенесенные инфекции, радиационное облучение, прием на ранних сроках беременности или незадолго до нее лекарственных препаратов, которые обладают тератогенным эффектом.
Что означают результаты?
Неделя беременности
Референсные значения
Источник: kdlmed.ru
Коротко о пренатальных генетических скринингах
Почти во всех странах мира беременным женщинам начали предлагать перинатальные (пренатальные) генетические скрининги, которые не являются обязательными для прохождения, но желательными, и я по ходу этой статьи объясню почему. «Наших» женщин пугают в первую очередь два слова в названии этих тестов: перинатальный и генетический. Дословно «перинатальный» означает «до рождения», то есть до рождения ребенка, и охватывает период беременности. Слово «генетический» имеет связь с генами, генетикой, однако не означает, что после пренатального генетического теста вам необходимо будет идти на консультацию к генетику. Часто врачи посылают женщин к генетику после сдачи этих тестов, потому что понятия не имеют, как интерпретировать результаты, но и сами генетики в большинстве случаев не знают.
Пренатальные скрининги (тесты) созданы с целью прогностического определения риска поражения плода рядом хромосомных аномалий и пороков развития. Это не диагностические тесты, поэтому они не могутзаменить диагностические методы обследования. Пренатальные скрининги обычно включают три основных параметра, которые учитываются при подсчете риска поражения плода рядом серьезных заболеваний: возраст матери, размеры воротникового пространства эмбриона, биохимические маркеры сыворотки крови беременной женщины.
В крови беременной женщины есть несколько веществ (маркеров), уровень которых меняется в зависимости от состояния плода и осложнений беременности. Комбинация этих маркеров и показатели их уровней могут быть прогностическим критерием в определении синдрома Дауна, пороков развития нервной трубки (спина бифида), передней стенки живота и ряда других заболеваний. Каждое медицинское учреждение использует свою комбинацию маркеров и имеет свои прентальные срининговые программы для беременных женщин, однако различие между такими программами незначительное. Все тесты делятся на скрининг первого триместра, который проводится до 14 недель беременности, и скрининг второго триместра, который проводится в 15-18 недель. Часто определение специфических маркеров может проводиться и в околоплодных водах на более поздних сроках беременности.Некоторые учреждения используют комбинацию скринингов первого и второго триместров.
Еще несколько лет тому назад пренатальный генетический скрининг предлагали пройти беременным женщинам возрастом 35 лет и старше, так как у них в несколько раз выше риск поражения плода синдромом Дауна, чем у женщин 20-25-летнего возраста. Сейчас пренатальный скрининг рекомендуется проходить всем беременным женщинам, независимо от возраста.
Существует несколько биохимических маркеров, которые определяют в сыворотке крови. Одни из них вырабатываются плацентой (ХГЧ, РАРР-А, ингибин А), другие – плодом (альфафетопротеин), третьи могут вырабатываться и плодом, и плацентой (эстриол 3). Эти маркеры появляются на разных сроках беременности, и их уровень меняется с прогрессом беременности, поэтому важно проводить такие скрининги вовремя, то есть на том сроке беременности, для которого эти скрининги были разработаны. Поспешное проведение на ранних сроках, или запоздалое на более поздних сроках может привести к получению ложных результатов.
Получив на руки результат, женщина либо нуждается в дополнительном обследовании, либо ничего предпринимать не нужно. Если вы получили результат и его данные выражены в количественных единицах, то есть указан уровень того или иного маркера, такие анализы не имеют практического значения.
Некоторые врачи «умудряются» посмотреть таблицы уровней, например, ХГЧ, и, сверив цифры, определяют срок беременности. Но при чем здесь срок беременности и пренатальный скрининг, который не проводится с целью определения срока беременности? Только при том, что проводить этот скрининг необходимо строго в рамках сроков беременности, когда его результаты имеют максимальную достоверность. Точный срок беременности должен быть известен до проведения скрининга, а не наоборот!
Правильный результат анализа содержит заключение о шансе плода быть пораженным синдромом Дауна или пороком развития нервной трубки, и этот шанс выражается не в процентах, а в пропорции. Например, 1:200, 1:3456 и т.д. Это означает, что шанс того, что у ребенка может быть такая-то проблема с учетом всех факторов и показателей маркеров, один на 200 случаев нормальной беременности.
Чем больше показатель, тем меньший риск поражения плода. Поэтому 1: 3456 намного лучше, чем 1: 200.Дальше врач должен сравнить показатели женщины с показателями возрастной категории местности, в которой она живет или проходит обследование. Обычно в заключении лаборатории есть такое сравнение и говорится, что риск высокий, средний или низкий. Если риск такой же возрастной группы женщин составляет 1: 500, например, а у женщины показатель 1:1000, то это означает, что риск поражения плода очень низкий – ниже, чем у большинства беременных женщин ее возраста данной местности. Если, наоборот, у женщины показатель 1:250 по сравнению с групповым, то риск будет средним или высоким.
В спорных ситуациях должны учитываться все факторы, в том числе показатели УЗИ, данные семейной истории и другие. Поспешное прерывание беременности только на основании результатов пренатального скрининга является ошибкой. Дело в том, что ложноположительный тест может быть при неправильном вычислении срока беременности (например, у женщины 16 недель беременности, а врач ошибочно поставил ей 14 недель, и все результаты сверяются с этим сроком беременности); при многоплодной беременности количество маркеров вырабатывается больше, и ряде других случаев показатели могут быть повышены. Индивидуальный подход в интерпретации результатов анализа позволит избежать многих поспешных выводов, а значит, и грубых ошибок.
P.S. Я советую всем женщинам, проживающим на территории бывших стран Союза, перед тем, как идти в лабораторию сдавать кровь на генетический скрининг первого или второго триместра, позвонить в лабораторию и спросить:
1.Проводит ли ваша лаборатория компьютерное вычисление индивидуального риска поражения плода синдромом Дауна и рядом других проблем, на основании уровня тех маркеров (веществ), которые вы определяете в крови этим скринингом?
Если ответ «Да» – второй вопрос:
2. Как выражается заключительный результат такого исследования, т.е. как звучит заключение?
Правильный ответ: в виде пропорции, например, один к такому-то числу. Если ответ «Нет» или в отношении заключительного результата дремучий лес, не спешите тратить деньги, а лучше сохраните их на что-то более полезное.
Поделиться ссылкой:
- Нажмите, чтобы поделиться в WhatsApp (Открывается в новом окне)
- Нажмите, чтобы поделиться в Telegram (Открывается в новом окне)
- Нажмите, чтобы открыть на Facebook (Открывается в новом окне)
- Нажмите, чтобы поделиться на Twitter (Открывается в новом окне)
- Нажмите, чтобы поделиться в Skype (Открывается в новом окне)
- Послать ссылку другу по электронной почте (Открывается в новом окне)
- Нажмите для печати (Открывается в новом окне)
Источник: doctorberezovska.com