ФЕНОЛЫ
ФЕНОЛЫ — органические соединения ароматического ряда, содержащие в молекуле одну или несколько гидроксильных групп, связанных с атомом углерода ароматического ядра. Фенолы и продукты их превращений являются природными эндогенными антиоксидантами (см. Антиокислители) в растительных и животных клетках.
Эти соединения обладают бактерицидными свойствами, в медицине используются для дезинфекции (см. Дезинфицирующие средства) и в качестве лекарственных средств с антисептическим действием (см. Антисептические средства). В медицинской и пищевой промышленности фенолы используют в качестве консервантов.
Многие синтетические производные фенола (простые эфиры, галоидные производные и др.) применяют для самых различных целей, например ксероформ — как антисептическое средство, дифениловый эфир — как теплоноситель, нитропроизводные (пикриновая кислота и др.) являются взрывчатыми веществами. Фенолы служат исходным сырьем для промышленного синтеза многих лекарственных средств, пластмасс, красителей. Многоатомные фенолы применяют в качестве антиоксидантов в фармацевтической, пищевой и парфюмерной промышленности, проявителей в фотографии, как стабилизирующие, консервирующие добавки в химические и нефтехимические промышленности. Некоторые фенолы токсичны: на производствах, связанных с их получением или использованием, они могут представлять профессиональную вредность.
ФЕНОЛ

По числу гидроксильных групп, присоединенных к бензольному кольцу (см. Бензол), фенолы делят на одно-, двух- и трехатомные. Первым представителем ряда фенолов, по которому названа вся группа этих соединений, является фенол, оксибензол, или карболовая кислота (см.); двухатомные фенолы — пирокатехин, или о-диоксибензол, гидрохинон (см.), или n-диоксибензол, резорцин (см.), или м-диоксибензол; трехатомные фенолы — пирогаллол (см.), или 1,2,3-триоксибензол, оксигидрохинон, или 1,2,4-триоксибензол, флороглюцин, или 1,3,5-триоксибензол. К фенолам относятся крезолы (см.) — оксипроизводные толуола (см.), ксиленолы — оксипроизводные ксилолов (см.).
В природе фенолы редко встречаются в свободном виде. В растениях они содержатся в виде различных производных, например, эвгенол — в гвоздичном масле, сафрол — в сассафросовом масле. Особенно много производных фенола в плодах цитрусовых. В небольших количествах фенолы присутствуют во всех плодах и фруктах. С пищей человек получает в сутки около 50 мг фенолов.
Фенолы в подавляющем большинстве являются бесцветными кристаллическими веществами, одноатомные фенолы обладают характерным интенсивным запахом, легко отгоняются с водяным паром. Многие фенолы хорошо растворимы в воде и бензоле, все фенолы хорошо растворяются в спирте. Фенолы обладают кислотными свойствами, реагируют со щелочами, образуя соли (феноляты).
На этом свойстве основано выделение фенолов методом экстрагирования каменноугольной смолы растворами щелочей или аммиачной водой. Фенолы проявляют также химические свойства оксисоединений (образуют простые и сложные эфиры), а также свойства соединений ароматического ряда. Фенолы легко окисляются.
Их способность к окислению возрастает по мере увеличения числа гидроксильных групп в ароматическом ядре. Реакция окисления фенолов имеет очень большое значение в химии и биохимии этих соединений. В промышленности фенолы получают экстрагированием каменноугольной смолы, некоторые простые фенолы (карболовая кислота, резорцин, гидрохинон) получают синтетически.
В организме человека фенолы полностью окисляются или инактивируются другим путем (напр., путем метилирования). Не исключено, что фенолы, поступающие с пищей, используются для биосинтеза полифенолов: катехоламинов (см.), иидолиламинов, убихинонов (см. Коферменты).
Фенолы как профессиональная вредность
Фенолы могут поступать в организм людей, работающих в контакте с ними, через легкие, неповрежденную кожу и слизистые оболочки. Из организма человека фенолы выделяются с мочой (небольшая часть — с выдыхаемым воздухом), главным образом в виде конъюгатов с серной и глюкуроновой кислотами. Одноатомные фенолы, в том числе крезолы, ксиленолы и др., являются нервными ядами, действующими на центральную нервную систему, они также оказывают сильное прижигающее и раздражающее действие на кожу.
Галогенопроизводные одноатомных фенолов, в особенности ди- и трихлорфенолы, а также гексахлорфен (2-2′-диокси -3,5,6,3′,5′,6′-гексахлордифенилметан) могут в процессе производства и при реакции разложения образовывать исключительно токсичные диоксины, из которых наиболее известен 2,3,7,8-тетрахлордибензо-n-диоксин, или ТХДД. Диоксины даже в очень малых количествах проявляют дерматотоксические, гепатотоксические и нейротоксические свойства с отдаленным воздействием на генотип.
Многоатомные фенолы проявляют свойства кровяных ядов, вызывая образование метгемоглобина (см. Метгемоглобинемия), гемолиз (см.) с развитием гемолитической желтухи (см.). Из многоатомных фенолов очень токсичным является пирокатехин (наиболее токсичный из диоксибензолов). Резорцин (м-диоксибензол) менее токсичен, чем другие диоксибензолы, несмотря на выраженное резорбтивное действие. Пирогаллол, используемый в фармацевтической промышленности как исходный продукт для синтеза некоторых противоглистных средств (см.), вызывает образование метгемоглобина, очень токсичен.
При судебно-медицинском исследовании трупов людей, умерших от отравления фенолом, отмечают изменения, аналогичные изменениям, описанным при отравлении карболовой кислотой.
Картину хронического и острого отравления, первую помощь, неотложную терапию, лечение, профилактику отравлений фенолами — см. Карболовая кислота.
Препараты фенолов
К применяемым в медицинской практике препаратам фенола относят карболовую кислоту, трикрезол и другие крезолы, лизол (см.), резорцин (см.), а также фенилсалицилат (см.), при метаболизме которого в организме образуется фенол. Кроме того, фенолы являются действующим началом некоторых природных продуктов, например, березового дегтя (см. Дегти), используемых в качестве лекарственных средств.
Препараты фенола губительно влияют практически на все виды микроорганизмов (бактерии, простейшие, вирусы и др.), что обусловлено, по всей вероятности, способностью этих препаратов вызывать денатурацию белков. При нанесении на кожу в соответствующих концентрациях: препараты фенола оказывают местно-раздражающее и даже прижигающее действие. Отдельные препараты фенолов (резорцин, деготь березовый) при; местном применении вызывают кератопластический и кератолитический эффекты (см. Кератолитические, кератопластические средства).
В медицинской практике препараты фенола используют главным образом как антисептические и дезинфицирующие средства. Некоторые препараты (например, фенол, трикрезол) применяют для консервации вакцин, сывороток и инъекционных лекарственных форм. В качестве антисептиков в стоматологической практике применяют главным образом резорцин и трикрезол. Препараты фенола с кератолитическими и кератопластическими свойствами (резорцин, деготь березовый) используют местно при лечении ряда кожных заболеваний (себореи, экземы и др.). Фенилсалицилат применяют внутрь, (обычно в сочетании с другими препаратами) при заболеваниях кишечника (колитах, энтероколитах) и мочевых путей (пиелитах, пиелонефритах, циститах).
Побочное действие препаратов фенола при местном применении проявляется в основном признаками локального раздражения тканей.
Препараты фенола, отличающиеся высокой липофильностью (фенол, трикрезол), легко всасываются через кожу и слизистые оболочки (особенно при их повреждении), в связи с чем такие препараты даже при местном применении могут оказать неблагоприятное резорбтивное действие на организм и вызывать токсические явления (головокружение, головную боль, общую слабость, нарушения дыхания, снижение АД и др.).
По степени токсичности для человека препараты фенола отличаются друг от друга. Наиболее высокой токсичностью при приеме внутрь обладает фенол (карболовая кислота), наименее токсичен фенилсалицилат.
При приеме внутрь препараты фенола (кроме фенилсалицилата) могут вызывать острые отравления (см. Отравления, таблица).
Библиогр.: Барабой В. А. Биологическое действие растительных фенольных соединений, Киев, 1976; Биохимия фенольных соединений, под ред. Дж. Хар-борна, пер. с англ., М., 1968; Глазова О. И. Отравления и первая помощь при них, с. 55, М., 1944; 3 а п р о м ет о в М. Н. Основы биохимии фенольных соединений, М., 1974; Л у д е в и т Р. и Л ос К. Острые отравления, пер. с нем., с. 370, М., 1983; Малышева В. В. и др.
Физиолого-гигиеническая характеристика условий труда и состояние здоровья рабочих в производстве фенолов методом полукоксования углей, Гиг. труда и проф. заболев., № 1, с. 18, 1967; М а ш к о в с к и й М. Д. Лекарственные средства, ч. 2, с. 404, М., 1984; Неотложная помощь при острых отравлениях, под ред. С. Н. Голикова, с. 174, М., 1977; Профессиональные болезни, под ред. А. А. Летавета, с. 306, М., 1973; Степанов А. В. Судебная химия (химикотоксикологический анализ) и определение профессиональных ядов, с. 112, 220, М., 1951; Ш в а й к о в а М. Д. Токсикологическая химия, с. 111, М., 1975.
3. А. Волкова (гиг.), В. К. Муратов (фарм.), Н. В. Проказова (биохим.).
Источник: xn--90aw5c.xn--c1avg
Что такое фенол и насколько он вреден для здоровья

МОСКВА, 9 декабря, ФедералПресс. Экологи сегодня утром зафиксировали повышение концентрации фенола в Химках возле OBI. Рассказываем, что это за вещество, чем опасно для здоровья и кто страдает от фенола чаще всего.
Фенол, или гидроксибензол – органическое соединение, простейший представитель класса фенолов. Выглядит как бесцветные игольчатые кристаллы, которые в воздухе из-за окисления розовеют. Запах фенола в высокой концентрации схож с запахом гуаши.
Это высокоопасное вещество – II класс опасности. К таким же веществам еще относят, например, формальдегид и сероводород.
Для фенола установлены ПДК. Предельно допустимая максимально-разовая концентрация – 0,01 мг/м³. Предельно допустимая концентрация в атмосферном воздухе среднесуточная – 0,006 мг/м³.
Опасность фенола
Фенол – сильный ирритант. Это значит, что пары вещества раздражают слизистую и дыхательные пути, а растворы вызывают сильные ожоги.
При вдыхании воздуха с парами фенола большая часть вещества быстро поступает в легкие. Высокие дозы фенола могут вызывать чихание, кашель, головокружение, головную боль. Длительное вдыхание обернется серьезными расстройствами нервной системы, нарушением работы дыхательных органов и даже сердца.
Где встречается вещество
Фенол активно выделяется при горении древесины. Также содержится в выбросах промышленных производств и выхлопных газах. В России чаще всего на фенол жалуются жители крупных промышленных городов, например Омска.
В быту источники выбросов фенола – смолы. Их используют для производства стройматериалов – ламината, фанеры, теплоизоляции, а также мебели из фанеры, ДСП и МДФ. Само по себе присутствие фенола не критично. Но если производитель стройматериалов или мебели не особо тратился на свою продукцию и нарушал стандарты, то парами фенола можно отравиться.
Но фенол – это не только вредные и удушающие выбросы. Вещество используют в медицине: он есть в антисептиках и дезинфицирующих средствах. Производные фенола содержатся в жаропонижающих препаратах, например в парацетамоле.
Ранее экологи зафиксировали превышение концентрации фенола в воздухе вблизи горящего OBI в Химках. «ФедералПресс» приводил оценку ПДК от минэкологии Московской области здесь.
Фото: ФедералПресс / Полина Зиновьева
Подписывайтесь на ФедералПресс в Дзен.Новости , а также следите за самыми интересными новостями в канале Дзен . Все самое важное и оперативное — в telegram-канале « ФедералПресс ». Также присоединяйтесь к нам в соцсетях: мы есть в Telegram , ВКонтакте и Одноклассниках .
Источник: fedpress.ru
Свойства фенола и его влияние на организм человека
Фенол является простейшим представителем веществ, которые относятся к классу фенолов или так называемых ароматических углеводородов. Чаще всего это вещество используется для нужд строительства, производства органических материалов (пластмассы) и химической промышленности. Также он востребован и в других отраслях науки, в том числе в медицине и сельскохозяйственной химии.
Основные характеристики вещества
В 1834 году, в процессе перегонки каменноугольных смол было открыт фенол, причём его не синтезировали, как некоторые другие вещества, а выделили из угольных пластов. За более чем полтора века вещество успело поменять название (старое название — «карболовая кислота», химики до сих пор называют его «карболка»).
На сегодняшний день наименование химического соединения, к которому относится фенол — гидроксибензол. Со временем были уточнены некоторые физические свойства фенола, которые в XIX веке установить без погрешностей было проблематично. Молярная масса фенола равна 94,11 г/моль, его плотность составляет 1.07 грамм на кубический сантиметр.
Интересно, что при температуре в 40,9 градусов по Цельсию вещество — которое в своём обычном агрегатное состоянии является кристаллическим — начинает плавиться, приобретая характерный оттенок. При обычной (комнатной) температуре фенол представляет собой небольшие кристаллы, не имеющие цвета. Эти кристаллы сильно пахнут гуашью, запах фенола очень специфичен и способен надолго «прицепляться» к предметам и одежде.
Способность гидроксибензола к образованию однородных систем с другими веществами (проще говоря, растворимость) не очень высокая, это вещество не может полностью раствориться в воде. Фенол, формула которого C6H5OH, является токсическим и едким веществом, относящимся к ирритантам — раздражителям слизистой оболочки и кожных покровов человека.
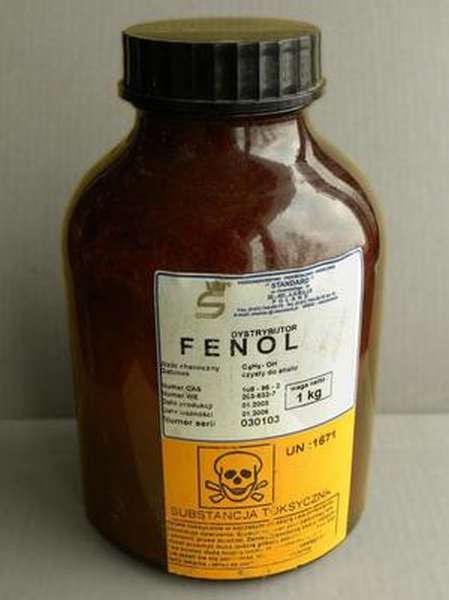
Ещё одна особенность фенола — в его сильных кислотных свойствах. Также он может вступать в реакцию с щелочными растворами, образуя феноляты или соли. При реакции с гидроксидом натрия (Na OH) образуется фенолят натрия (C6H5ONa). Для класса фенолов характерно сочетание химических свойств ароматических углеводородов и спиртов.
Значение предельно допустимой концентрации (ПДК) фенола для человека в жилой зоне составляет 0,03мг/м в кубе, для рабочей зоны это значение равно 0.3 мг/м в кубе. Являясь летучим веществом, фенол опасен при попадании через дыхательную систему человека, а также через кожу, на которой он оставляет химические ожоги. В некоторых случаях симптомы отравления фенолом можно спутать с аллергией, так как имеются похожие симптомы (в виде тошноты, рвоты, опухания кожи).
Использование в промышленности
Для промышленного производства чаще всего используют фенольные соединения, которые можно разделить на 4 небольших группы:
Прочтите также: Польза и вред натуральных и искусственных заменителей сахара
- Жидкости, получаемые посредством перегонки каменноугольного или древесного дёгтя. К примеру, лизол или креозот.
- Соединения, полученные в естественной среде (природные). К ним относят флавоноиды, эвгенол, лигнин, а также капсаицин.
- Хлорфенолы и бутилфенолы.
- Сама карболовая кислота.
Эти соединения получили обширное применение в различных сферах и отраслях. С помощь фенолов производят лакокрасочные изделия, которые имеют хорошую стойкость к воде и многим растворителям. Иногда для изготовления лаков используют алкилфенольные смолы, которые значительно увеличивают их срок службы.
Моющие средства, а также некоторые гели для уборки делают при помощи фенола. Однако в последнее время, в связи с новыми исследованиями, производители стараются отказываться от добавления в состав средства вредных для здоровья веществ. Фенол, наряду с хлором, кислотами и щелочами относится именно к таким веществам.
Широчайшее распространение получил фенола в производстве пластмассовых изделий, а также различных типов синтетических тканей (типа капрона и нейлона). Их делают при помощи синтетических фенолформальдегидных смол. Свойства, которыми обладает фенолформальдегид, позволяют этому материалу до сих пор оставаться востребованным и полезным:
- Высокие показатели электроизоляционных свойств.
- Устойчивость к сильным механическим нагрузкам.
- Превосходная коррозийная стойкость.
- Универсальность для использования.
Из этой синтетической смолы изготавливают много различных приспособлений, предметов и деталей по типу вилок, розеток, электроутюгов, электросчётчиков, выключателей, клеммных коробок и прочих электротехнических изделий.
Список можно дополнить абразивными инструментами, деталями военной техники и оружия, элементами бытовых и кухонных приборов, текстолитов, канцтоваров, различных связующих материалов, сувениров, шахмат и шашек, а также упоминаемых выше лаков и клеёв.
Применение в медицинской сфере
В медицине довольно часто применяют средства, которые могут быть очень опасны для человека, если, к примеру, неправильно заклеить рану или превысить дозу препарата. Примером таких средств может служить цианистый акрилат (ЦА), а также фенол и похожие на него вещества.
Класс фенолов имеет высокие бактерицидные свойства, которые активно используют для обеззараживания медицинских инструментов и помещений. При растворении 5% фенола в воде получается антисептический раствор, хорошо себя зарекомендовавший для обработки ран.
В силу своей токсичности, фенол применяют для дезинфекции только в смесях с другими веществами и средствами. Часто для дезинфицирующих мероприятий используют фенольный раствор, в котором содержится калийное мыло, благодаря чему возможно замачивать бельё и обеззараживать помещения без особого вреда для здоровья человека.
Применение фенола также нашло себя и в лечении некоторых кожных заболеваний, таких, как кондиломы (папилломы), фолликулиты, фликтена, сикоз, импетиго, пиодермия и гнойные раны. Для таких процедур используют, как правило, глицериновый раствор фенола. Тем не менее при таком лечении могут быть побочные эффекты в случае попадания препарата в дыхательные пути.
Прочтите также: Симптомы и первая помощь при отравлении этиловым спиртом
Помимо прочего, фенол является необходимым компонентом для препаратов, которыми пользуются люди на протяжении длительного времени. К ним можно отнести следующие лекарства:
- Аспирин. После получения аминосалициловой кислоты из фенола (на латыни — Acidum Aminosalicylicum), аспирин стал широко распространён, так как стало возможным наладить его производство в промышленных масштабах.
- Пурген. Такое вещество, как фенолфталеин (латинское название — Phenolphthaleinum) входит в состав Пургена и многих других эффективных слабительных.
- Противотуберкулёзные препараты, изготовленные на основе парааминосалициловой кислоты, которая тоже является производной фенола.
- Фукорцин. Противогрибковое средство, имеющее в своём составе до 40 мг фенола. Это лекарство также может использоваться при лечении стрептодермии, ветрянки, герпеса, лишая и подобных заболеваний.
- Ксероформ. Его могут назначить при хронической диарее, колитах и энтероколитах, а также при наличии других воспалительных процессов кожи и слизистой оболочки.
В последнее время набирает популярность фенолового пилинга лица и кожи. Это одна из процедур омоложения, которое достигается за счёт химического прижигания некоторых кожных участков с помощью фенола. Этот процесс способствует развитию регенерации и, как следствие, появлению новых молодых клеток.
Востребованность в сельском хозяйстве
Токсичные особенности фенольных веществ используют при борьбе с насекомыми-вредителями, а также против сорняков и паразитов. Инсектицидные средства на основе фенола обладают высокими обжигающими свойствами, благодаря которым также есть возможность лечить некоторые заболевания растений.
Учитывая современные разработки в области пестицидов, инсектицидов и прочих химических средств, фенол для сельскохозяйственных нужд используется значительно реже, чем прежде. Это объясняется не только потенциальным вредом для человека и животных, но и ввиду наличия более эффективных веществ.
К пестицидам на фенольной основе следует отнести все препараты, имеющие в своём составе 2,4-Дихлорфеноксиуксусную кислоту: Клопэфир, Дикопур, Антал, Альянс, Диамакс, Килео и другие.
Следует учитывать, что эти средства вредны для пчёл, поэтому вблизи пасеки их лучше не использовать.
Вред для здоровья человека
Отравление организма вследствие вдыхания паров фенола наступает очень быстро, за счёт чего можно без труда определить основные признаки интоксикации. При сильной концентрации вещества может наступить летальный исход либо же серьёзное поражение нервной системы, головного мозга и дыхательных путей.
Для взрослого человека такая смертельная доза может равняться всего одному грамму. В целом имеет смысл разделить симптомы отравления на две группы:

- Видимые признаки. Их возникновение говорит о большой концентрации ядовитого вещества, попавшего в организм пострадавшего человека. К ним относятся потеря сознания, сильная рвота, дезориентация человека в пространстве, заметное изменение цвета кожи, затруднённое дыхание (или удушье), несвязная речь. Человек слабо реагирует на внешние стимулы.
- Признаки, возникающие со временем. Возникновение диареи либо запоров, тошноты, головокружения, приступов мигрени (сильные головные боли), частые «неполадки» с желудком, постепенное изменение цвета кожи, появление волдырей, красных пятен. Нарушается работа дыхательной системы, может ощущаться сильное жжение в области груди, невозможность долгой задержки дыхания (не более 5−7 секунд).
Чаще всего подобные отравления происходят на химических фабриках и заводах. Нужно помнить, что если в воздухе рабочего присутствуют смеси различных химических веществ (не только фенол) — влияние на организм человека будет пагубным, даже при отсутствии признаков отравления. Нарушение техники безопасности никогда не приводит к хорошим последствиям.
Опасность, помимо заводов и фабрик, могут представлять лекарства, содержащие фенольные вещества либо же вдыхание паров бытовой химии (при уборке, к примеру). По этой же причине специалисты рекомендуют тщательно проветривать помещения после их покраски, особенно учитывая то, что в гидроксибензол довольно часто используется в лакокрасочной промышленности.
Плюс ко всему возможны несчастные случаи отравления фенолом, предугадать которые попросту невозможно. Именно поэтому следует знать, что надо делать в таких ситуациях.
Алгоритм действий при отравлении фенолом
Ядовитое вещество может попасть в организм 2 путями — через кожные покровы (фенол хорошо всасывается в кожу, после чего оказывает влияние на работу головного мозга) и через дыхательную систему. При вдыхании этот яд оказывает воздействие на дыхательную систему и способен остановить процесс дыхания, поэтому перво-наперво необходимо изолировать пострадавшего от отравляющего источника.
После чего нужно срочно звонить в скорую помощь. После чего следует открыть все форточки (если в помещении) или же снять верхнюю одежду пострадавшего для обеспечения свежего воздуха. Если яд попал через рот человека, нужно дать ему воды для полоскания. Эту воду глотать нельзя — она необходима только для смачивания поражённых участков слизистой оболочки рта.
Обработка поражённых участков кожи должна выполняться строго водой, недопустимы никакие спиртосодержащие жидкости, мази, масла и жирные вещества. Если с собой есть какой-либо вид сорбентов, следует дать человеку его выпить. Для этой цели подойдут такие препараты, как энтеросгель, полисорб, лактофильтрум, и, само собой, активированный уголь.
В качестве антидота к фенолу используют 10% раствор глюконата кальция (как правило, внутривенно). Однако следует заметить, что если человек никогда в жизни не делал никому инъекции, то лучше будет дождаться приезда врачей, где в токсикологическом отделении пострадавшему окажут необходимую помощь.
Источник: dlja-pohudenija.ru
Фенолы — строение, общая характеристика и основные свойства

Фенолы – органические соединения. Они в небольших количествах есть в природе. Основную массу фенола и производных на его основе получают синтетическим путём.
Что такое фенол
К фенолам относят производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с фенил радикалом. Они могут иметь одну или несколько гидроксогрупп.
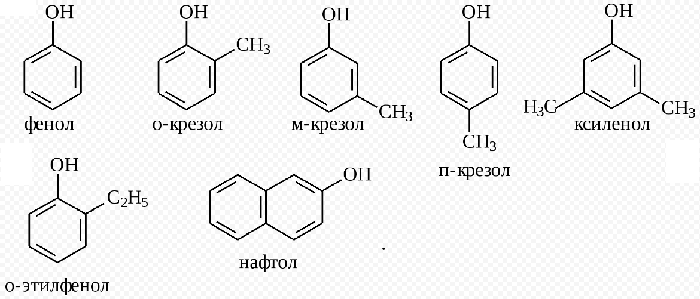
Самым простым представителем этой группы соединений считают фенол. Он и дал название классу веществ. Это же соединение называют гидроксибензолом.
Общая и структурная формулы
Состав веществ можно выразить общей формулой С6Н6-n(ОН)n.
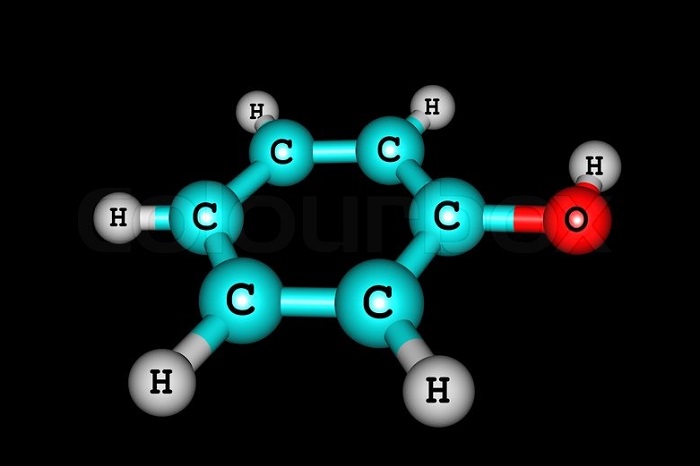
Простейший представитель класса имеет 1 гидроксогруппу. Его молекулярная формула С6Н5ОН. Структурная формула — ОН. Если в молекуле фенола 1 атом водорода заместить на метильный радикал, получим метилфенол. Если к нему прибавить ещё одно бензольное ядро, получим нафтол.
Химические свойства фенола
Так как гидроксибензол содержит в своём составе 2 группы атомов, выделяют две группы химических свойств.
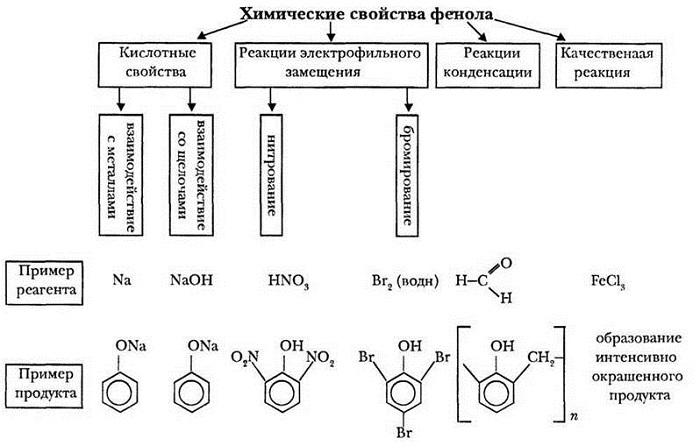
- галогенирование;
- нитрование;
- гидрирование;
- реакция поликонденсации.
Свойства, протекающие за счёт гидроксильной группы (кислотные свойства):
- диссоциация;
- взаимодействие с активными металлами;
- взаимодействие со щелочами.
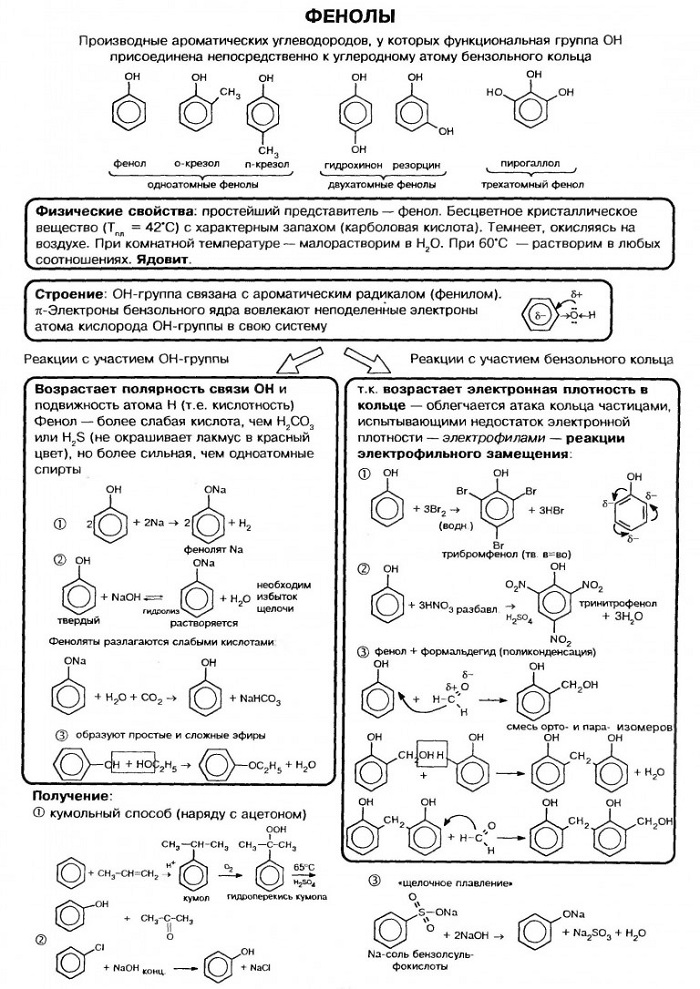
Не следует понимать, что фенол, имея в своем составе черты строения бензола и спиртов, просто повторяет их свойства. На самом деле все сложнее. Чтобы понять особенность его химических взаимодействий, необходимо знать строение вещества. В молекуле фенола наблюдается взаимное влияние атомов.
На атоме кислорода гидроксильной группы есть 2 неподелённые электронные пары. Они взаимодействуют с π – электронной системой фенил радикала.
Результат взаимодействия следующий:
- Нарушается равномерное распределение электронной плотности в фенил радикале. Она возрастает на атомах 2,4,6, то есть в орто– и параположениях. Именно в этих положениях водород будет легко замещаться на другие атомы.
- Атом водорода гидроксогруппы, из-за влияния фенил радикала, приобретает положительный заряд и становится более подвижным.
Результатом влияния служат своеобразные свойства фенола. Он реагирует с активными металлами и щелочами. Спирты – только с металлами. В то же время и бензол, и гидроксибензол реагируют с бромной водой. Но у фенола, в отличие от бензола, идет замещение сразу по 3 атомам.
Физические свойства
С6Н5ОН – это белое кристаллическое вещество. В результате окисления кристаллы могут приобретать розовый цвет. Температура плавления 40,9 0 С. Молярная масса 94 г/моль.

В холодной воде фенол является малорастворимым веществом. При температуре выше +70 0 С растворяется хорошо. Карболовая кислота – так называют водный раствор фенола. Лучше растворяется в органических растворителях.
Отличается характерным резким запахом. Вещество ядовито. Проникая в организм человека, вызывает тяжёлое отравление.
С чем реагирует фенол
Гидроксибензол вступает в реакцию с активными металлами. С натрием даёт фенолят натрия. Уравнение выглядит следующим образом:
2 С6Н5ОН + 2Na = 2С6Н5ОNa + H2
В реакциях со щелочами также образует феноляты. Реагируя с гидроксидом калия, образует фенолят калия:
С6Н5ОН + KOН = С6Н5ОK +H2O
Взаимодействуя со спиртами, образует эфиры. Например, в реакции с бутанолом, получают простой эфир:
С6Н5 ОН + НО–С4Н9 = С6Н5–О–С4Н9 +Н2О
Из свойств, протекающих за счёт фенил радикала, можно отметить реакцию нитрования. Взаимодействие с HNO3 даёт 2,4,6 тринитрофенол (пикриновую кислоту):
С6Н5ОН + 3HNO3 = C6H2(NO2)3OH +3H2O
Реагируя с формальдегидом, фенол образует фенолформальдегидную смолу. Это реакция поликонденсации – получение высокомолекулярного вещества из низкомолекулярных веществ с отщеплением побочного продукта. В данном случае – это вода.
Качественные реакции на фенол
К качественным реакциям относят взаимодействие с бромной водой. В результате получают осадок белого цвета:
С6Н5ОН + 3Br2 = C6H2Br3ОН + 3HBr
Ещё одной качественной реакцией является взаимодействие с хлоридом железа(III). Получается фиолетовое окрашивание. Качественные реакции позволяют разделить и определить органические вещества.
Реакция присоединения
К реакциям присоединения относят гидрирование ароматического ядра. Гидрирование – это реакции присоединения водорода. Превращение протекает легко, в присутствии катализатора. В результате разрушается π – электронная система, образуется циклогексанол и циклогексанон:
2С6Н5ОН + 5Н2 = С6Н11ОН + С6Н10О
Окисление
Фенол не устойчив к окислению. Продукты реакции могут быть разными. Это зависит от самого окислителя и от условий, в которых протекает реакция. При окислении перекисью водорода получается двухатомный фенол:
С6Н5ОН + Н2О2 = С6Н4(ОН)2
К реакции окисления относят и реакцию горения. Образуется углекислый газ и вода.
Получение фенола
Фенол в небольшом количестве содержится в каменноугольной смоле. Но потребности в веществе настолько велики, что этого источника недостаточно.
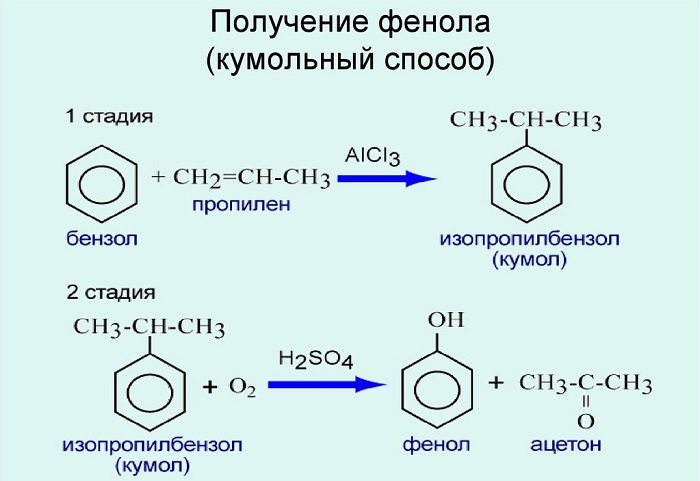
Разработаны разные способы получения:
Применение
Вещество применяют для производства разнообразной продукции:
- фенолформальдегидных смол и пластмасс;
- лекарственных препаратов;
- взрывчатых веществ;
- красителей;
- раствор фенола в воде обладает антисептическими свойствами;
- искусственных волокон и другой продукции.
Заключение
Фенол и фенольные соединения – очень важная группа веществ. Не следует забывать, что многие из них являются ядами. Все отходы промышленности, содержащие вещество, тщательно очищаются. Их подвергают каталитическому окислению, обработке озоном и другим способам очистки.
Источник: nauka.club